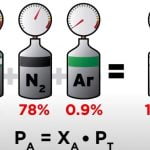
La ley de Dalton establece que la presión de una mezcla de gases que no interactúan entre sí, equivale químicamente a la suma de las presiones parciales de estos gases.
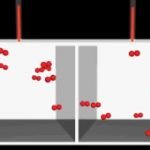
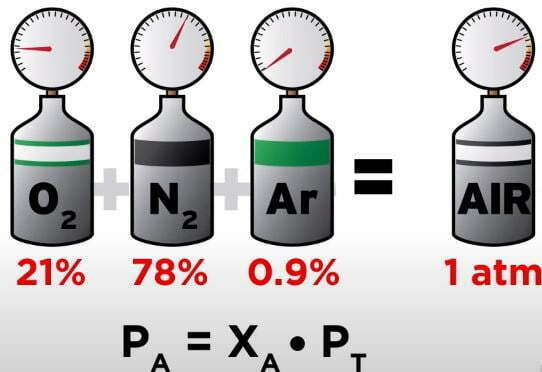
El aire en una habitación o local donde nos encontremos es una mezcla de varios gases, principalmente nitrógeno (alrededor del 78%) y oxígeno (alrededor del 21%) ver ejemplo de la imagen siguiente. La presión parcial de cada uno de estos gases es la presión que tendría el gas si ocupara todo el volumen solo. Por ejemplo, si todos los gases excepto el nitrógeno fueran retirados de la habitación, la presión de lo que queda sería una presión parcial de nitrógeno. La ley de Dalton establece que la presión total de todos los gases combinados equivalen a la cantidad de las presiones parciales de cada gas de una manera separada. Estrictamente hablando, la ley se aplica sólo a los gases ideales, pero con una aproximación bastante buena también describe los gases reales.
John Dalton formuló esta ley en 1801, aunque la teoría molecular-cinética de los gases (el modelo que describe el comportamiento de los gases) a partir de la cual fluye directamente, se desarrolló más tarde a mediados del siglo XIX. La presión del gas en las paredes del recipiente es el resultado de la colisión de moléculas de gas con estas paredes. Mirando el gas desde esta posición, es fácil entender que el número de colisiones con la pared de moléculas de cada tipo; dependerá de cuántas moléculas de este tipo estén presentes en el gas. Y de ello se deduce que la presión total, que es la suma de las colisiones de todas las moléculas, se obtiene mediante la adición del número de colisiones de moléculas de cada tipo.